| |
|
|
|
|
| |
|
|
КэАн»Ҝ№«КҪІйСҜ
6. »ҜС§ЖҪәвјЖЛ㹫КҪ ¶ФУЪҝЙДж·ҙУҰЈә ЈЁ1Ј©ёчОпЦКөДұд»ҜБҝЦ®ұИЈҪ·ҪіМКҪЦРПаУҰПөКэұИ ЈЁ2Ј©·ҙУҰОпөДЖҪәвБҝЈҪЖрКјБҝЈӯПыәДБҝ ЙъіЙОпөДЖҪәвБҝЈҪЖрКјБҝЈ«ФцјУБҝ ұнКҫОӘЈЁЙи·ҙУҰХэПтҪшРРЈ©Јә
ЈЁ3Ј©·ҙУҰҙпЖҪәвКұЈ¬·ҙУҰОпAЈЁ»тBЈ©өДЖҪәвЧӘ»ҜВКЈЁ%Ј©
ЛөГчЈәјЖЛгКҪЦР·ҙУҰОпёчёцБҝөДөҘО»ҝЙТФКЗmol/LЎўmolЈ¬¶ФУЪЖшМеАҙЛө»№ҝЙТФКЗL»тmLЈ¬ө«ұШРлЧўТвұЈіЦ·ЦЧУЎў·ЦДёЦРөҘО»өДТ»ЦВРФЎЈ ЈЁ4Ј©°ў·ьјУөВВЮ¶ЁВЙј°°ў·ьјУөВВЮ¶ЁВЙөДИэёцЦШТӘНЖВЫЎЈ ўЩәгОВЎўәгИЭКұЈә ўЪәгОВЎўәгС№КұЈә ўЫәгОВЎўәгИЭКұЈә ЈЁ5Ј©»мәПЖшМеөДГЬ¶И ЈЁ6Ј©»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝ ўЩ ЖдЦРMЈЁAЈ©ЎўMЈЁBЈ©ЎӯЎӯ·ЦұрКЗЖшМеAЎўBЎӯЎӯөДПа¶Ф·ЦЧУЦКБҝЈ»a%Ўўb%ЎӯЎӯ·ЦұрКЗЖшМеAЎўBЎӯЎӯөДМе»эЈЁ»тДҰ¶ыЈ©·ЦКэЎЈ ўЪ
|
||||||||||||||||||||
| ЙПТ»ТіЎЎЎЎПВТ»Ті | ||||||||||||||||||||
|
|
|||||||
 |
|||||||
|
°жИЁЛщУРЈә¶АЙҪФЪПЯ copyright ©2007-2025 www.dushan.net, All Rights Reserved
ұҫХҫОӘ№«ТжРФНшХҫЈ¬ЦјФЪРыҙ«¶АЙҪЈ¬ИфДъИПОӘОТГЗЗЦ·ёБЛДъөДИЁТжЈ¬ЗләНОТГЗБӘПөЈ¬ҫӯІйКөҪ«ј°КұёДХэ! email:webmaster#dushan.net   №у№«Нш°Іұё 52272602002010әЕ №ӨРЕІҝұё°ёЈәЗӯICPұё07001263әЕ №у№«Нш°Іұё 52272602002010әЕ №ӨРЕІҝұё°ёЈәЗӯICPұё07001263әЕ
|
|||||||




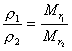 Ј¬јҙИОәОКұҝМ·ҙУҰ»мәПЖшМеөДГЬ¶ИУлЖд·ҙУҰ»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝіЙХэұИЎЈ
Ј¬јҙИОәОКұҝМ·ҙУҰ»мәПЖшМеөДГЬ¶ИУлЖд·ҙУҰ»мәПЖшМеөДЖҪҫщПа¶Ф·ЦЧУЦКБҝіЙХэұИЎЈ